FDA udzieliło oznaczenia na lek opracowany na bazie konopi do walki z padaczką u dzieci.
Chociaż FDA nie okazało pełnej aprobaty – twórca leku wciąż musi wykazać skuteczność leku w badaniach klinicznych – oznaczenie stanowi ogromny krok do przodu w dziedzinie medycyny opartej na konopi.

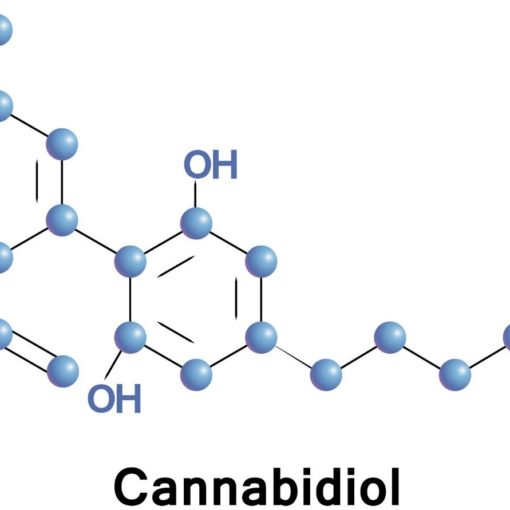
Lek o nazwie Epidiolex zawiera wysoko oczyszczoną, pochodzenia roślinnego formę kannabidiolu (CBD), niepsychoaktywnego związku znajdującego się w marihuanie, który nie wywołuje uczucia haju związanego z THC, główną substancją psychoaktywną rośliny. CBD jest od dawna stosowane w leczeniu zespołu Dravet, rzadkiej i ciężkiej postaci epilepsji u dzieci, a GW Pharmaceuticals przewiduje, że Epidiolex będzie przydatny zarówno w leczeniu zespołu Dravet oraz zespołu Lennoxa-Gastauta (LGS), innej rzadkiej postaci epilepsji u dzieci.
FDA przyznaje oznaczenie leku sierocego do leków przeznaczonych do leczenia rzadkich zaburzeń. To kwalifikuje się do przygotowania leku do pewnych ulg podatkowych związanych z badaniami klinicznymi, jak również okresu wyłączności obrotu leku.
Obecnie rząd federalny klasyfikuje marihuanę jako substancję Grupy 1, ale jej związki, takie jak CBD i THC, mogą zostać przekwalifikowane na niższy poziom ryzyka, jeżeli zostaną zatwierdzone do użytku medycznego przez FDA. Zatwierdzenie przez agencję syntetycznego THC w leku na jego bazie – Marinolu, w 1985 roku, spowodowało, że THC stało się substancją Grupy 3.